近日,康弘药业公告称,公司申报的3类仿制药利非司特滴眼液国内首家获批生产并视同过评,适用于治疗干眼(DED)的体征和症状。米内网数据显示,2024年中国三大终端六大市场眼科用药(化药+生物药)销售额超过200亿元。
利非司特滴眼液是由美国Shire Dev LLC(后被诺华收购)开发的第一代淋巴细胞功能相关抗原-1(LFA-1)拮抗剂,最早于2016年7月在美国获批上市,目前尚未获批进入国内市场。
2023年12月,国家卫健委等六部门发布了《第三批鼓励仿制药品目录》名单,利非司特滴眼液赫然在列。
目前已有多家药企布局利非司特滴眼液仿制药,康弘药业、齐鲁制药以新注册分类报产,其中康弘药业已于近日顺利获批,为国内首家;此外,鲁南贝特制药、辰欣佛都药业、杭州百诚医药、浙江莎普爱思药业等企业的产品获批临床。

康弘药业表示,本次利非司特滴眼液获批上市,丰富了公司眼科领域的产品管线,提升公司在眼科用药领域的市场竞争力。
米内网数据显示,近年来中国三大终端六大市场眼科用药(化药+生物药)的销售额逐年上涨,2023-2024年均超过200亿元。在一级集团排名中,诺华稳居首位,但占比呈下滑趋势;康弘药业位列第二,2024年市场份额超过11%。
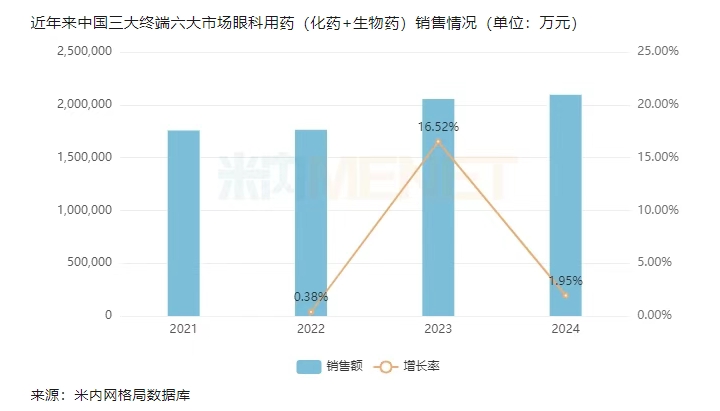
在眼科用药领域,康弘药业拥有4个品种的生产批文,其中康柏西普眼用注射液为公司核心产品,2024年在中国三大终端六大市场的销售额超过23亿元,在眼科用药(化药+生物药)品牌排名中稳居首位。
在研眼科1类新药中,KH631眼用注射液、KH658眼用注射液均处于I/II期临床,适应症分别为(湿性)年龄相关性黄斑变性、新生血管性(湿性)年龄相关性黄斑变性等;KH906滴眼液已完成I期临床,适应症为角膜新生血管。